半導体配線の主な目的は、電気信号を高速・確実に伝えることです。ですが微細化が進むにつれて、配線抵抗(R)と容積(C)との積であるRC積が増大し、信号遅延の要因となります(RC積についてはこちら)。
このRC積を低減するためには、以下のような設計の工夫が必要です。
- 低誘電率材料(Low-k膜)による容量Cの抑制
- 断面積を確保することによる抵抗Rの抑制(より細く深い配線構造=高アスペクト比構造)
ところがこの高アスペクト比構造は、ステップカバレッジ(成膜均一性)の悪化という新たな課題をもたらしました。
ステップカバレッジとは
ステップカバレッジ(step coverage)とは、基板上にあるトレンチやコンタクトホールなどの段差構造において、膜がどれだけ均一に形成されるかを示す指標です。特に、
- 側壁の被覆性(sidewall coverage)
- 底部の被覆性(bottom coverage)
が重要になります。
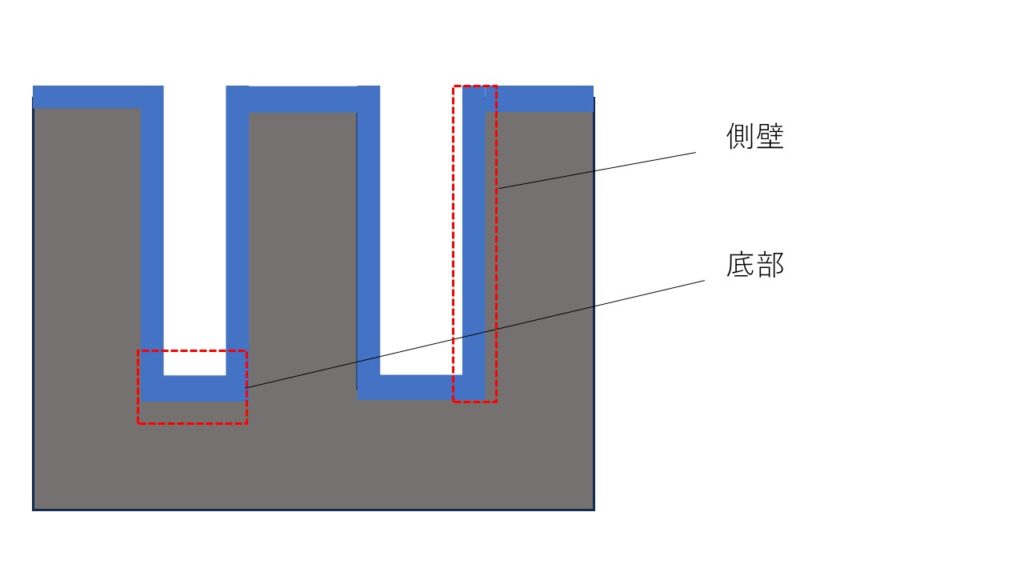
高アスペクト比構造では、成膜源(プリカーサー、precursor)が底部まで届きにくくなり、側壁や底部の膜厚が薄くなる傾向があります。
このような不均一な成膜は、絶縁不良・リーク・配線断線などの信頼性を低下させます。
成膜法における課題
では良好なステップカバレッジを実現するには、どのような成膜手法が適当でしょうか。
成膜法の比較:PVD・CVD・ALD
ステップカバレッジの課題を考える際には、主要な成膜手法の特徴を比較しておくことが有用です。
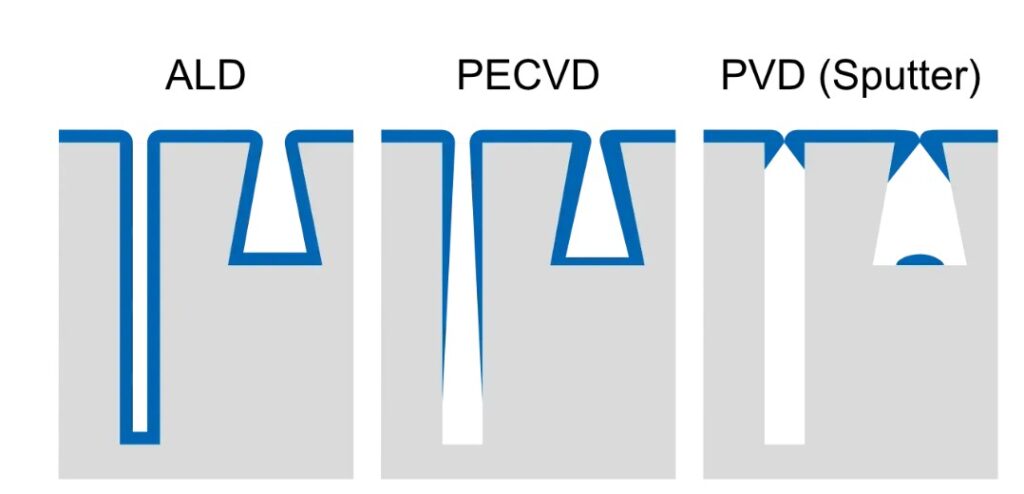
- PVD(物理気相成長):スパッタリングなどに代表される手法です。粒子が直進的に飛ぶため、トレンチ底部などへの堆積が難しく、ステップカバレッジが悪い。
- CVD(化学気相成長):ガスが拡散して回り込むため、ある程度のカバレッジは確保できるが、熱分解位置が早すぎると上部に偏る。
- ALD(原子層堆積):表面反応を制御でき、優れたステップカバレッジを持つが、成膜速度やコスト面での制約がある。
このように、CVDはスピードと均一性のバランスに優れる手法ですが、熱分解の位置を制御する工夫が重要となります。
参照:
「ステップカバレッジとは」菅製作所(https://agus.co.jp/?p=6853)
「化学気相成長(Chemical Vapor Deposition: CVD)法の基礎」(Journal of the Vacuum Society of Japan Vol59, No.7, 2016 11-17p)
CVD法の課題:プリカーサーの熱分解位置
CVDでは、ガス状のプリカーサー(前駆体)が基板表面に到達・吸着し、化学反応を経て固体膜を形成します。
しかし高アスペクト比構造では、次のような問題が発生します(上図参照)。
- プリカーサーがトレンチ底部に届く前に熱分解、
- その結果、トレンチ上部ばかりに成膜されてしまう。
つまり、届く前に分解してしまう、という現象が、不均一な成膜の正体です。
成膜パターンの比較
以下は、不均一な成膜の解消を示した図です。
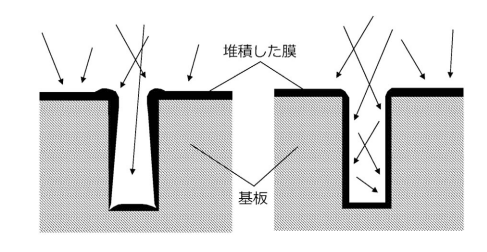
左図:プリカーサーの物質移動(拡散)段階が律速(熱分解が早く、上部ばかりに成膜)
右図:表面反応が律速(プリカーサーがトレンチの底部まで運ばれた後に反応し、均一に成膜)
図から分かるように、反応が始まるタイミング(熱分解位置)を制御することでステップカバレッジが改善できます。
※律速については、別の記事で扱います。
東京エレクトロンの工夫:CO分圧で届かせてから、反応させる
この課題に対して、東京エレクトロンの特許(特開2015-160963「ルテニウム膜の成膜方法および成膜装置、ならびに半導体装置の製造方法」)では、次のようにアプローチをしています。
- プリカーサーにルテニウムカルボニル(ruthenium carbonyl, Ru₃(CO)₁₂)を使用、
- COガスを付加的に導入することでCO分圧を高め、熱分解を制御
なお、この明細書では、バリア層としてのRu膜を、熱CVD法により成膜しています(プリカーサー Ru₃(CO)₁₂を熱分解し、金属Ruを析出、副生成物として一酸化炭素(CO)を放出)。
分解反応(可逆反応)
Ru3(CO)12(g) ⇌ 3Ru(s) + 12CO(g)
この反応は可逆反応であり、生成物であるCOの分圧を高めると、その変化を打ち消すように反応は左向き(Ru₃(CO)₁₂の熱分解の抑制)に進もうとします。
これはルシャトリエの原理によって説明できます。
原理の確認:ルシャトリエの原理
ルシャトリエの原理とは、
平衡状態にある系において変化(圧力・温度・濃度)を与えると、それを打ち消す方向に平衡が移動する、という法則です。
たとえば、生成物の濃度(または分圧)を高めると、反応は生成物を減らす方向(逆反応)へと進みます。
補足:分圧とは?
可逆反応における「濃度」に相当するものとして、気体では「分圧」が使われます。
分圧とは、「混合気体中の各成分のモル分率 × 全圧」
- 圧力:気体分子が容器の壁に衝突する強さ・頻度
- モル分率:全体の物質量(mol数)のうち、特定の気体の物質量(mol数)の割合(濃度)
たとえば、気体Aと気体Bの混合気体では、気体Aの分圧は「 Aのモル分率 × 全体の圧力」、つまりAの粒の割合に比例します。
なぜCOガスを追加するのか?
特許内では、プリカーサー供給時のキャリアガスのみではCO分圧が不十分であり、キャリアガスに加えて別に付加的COガスを導入することによって、Ru₃(CO)₁₂の分解位置をトレンチの下方(チャンバ内の下方)にシフトさせることが可能になります。
明細書では、Ru₃(CO)₁₂ / COの分圧比を0.0025以下に制御することが有効とされています。
成膜均一性の向上
このように、CO分圧の制御によって、Ru₃(CO)₁₂が深部まで届き、届いた表面で反応が進み、トレンチ底部を含む構造全体で均一な成膜が実現されます。
従来はプリカーサーが届かないことで成膜が不均一になっていたのに対し、分圧の調整により、届いてから反応させることが可能になり、良好なステップカバレッジ)が実現されます。
参考:
「化学気相成長(Chemical Vapor Deposition: CVD)法の基礎」(Journal of the Vacuum Society of Japan Vol59, No.7, 2016 11-17p)(再掲)



コメント