前回の記事「固体でも『拡散』する ― EUVミラーと水素の侵入」では、EUVリソグラフィ装置内で発生する水素ラジカルが、固体であるはずのEUVミラー多層膜内部に拡散し、内部で水素分子として再結合することでブリスタリングを引き起こすしくみについて解説しました。
この問題に対しては、2層構造の保護層が提案されましたが、それだけではブリスタリングを防げず、さらなる対策が必要でした。
そこで今回は、2層構造の限界を踏まえたうえで、「再結合層」という第3の工夫について整理します。
振り返り:2層構造
特許【WO2014139694】では、水素からの保護手段として保護層を2層構造とする提案がされていました。
第3層の設計意図を理解する前提として、前回の記事で紹介した2層構造を確認すると
- 第1層(下層):水素を通さない拡散の防止(水素溶解度が低い材料)
- 第2層(上層):水素を一時的に取り込んで吸収を抑制(水素溶解度が高い材料)
という役割分担により、外部の反応性水素の侵入を制御しています。
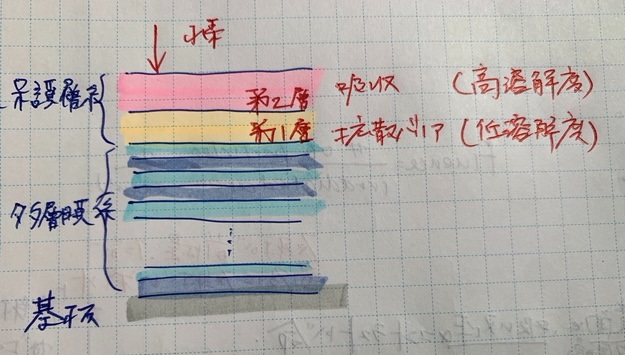
※明細書では、水素の溶解度とは「大気圧下で水素吸収材料100gに取り込まれる水素分子の体積(cm3)」と定義している。
2層構造の限界
第2層をすり抜けて第1層に到達した水素ラジカルは、その場で再結合し、水素分子(H₂)となります。
しかし、第1層は水素の溶解度が低くなるよう設計されているため、生成された水素分子を十分に溶解・拡散させることができません。その結果、第1層に水素分子が侵入してもこの水素分子の逃げ場がなく、内部に滞留してしまいます。
これがやがて内圧となって膨張し、ブリスタリングを引き起こします(この点については「低溶解度材料がブリスタしやすい理由」でも紹介しました)。
※明細書では再結合率を、表面で吸着された水素原子が再結合し水素分子を形成し、表面から除去されるか、を示す。
The recombination rate indicates how likely it is that hydrogen atoms adsorbed at the surface will recombine to form hydrogen molecules and be removed from the surface.
このように、2層構造では保護層内部で再結合が起こるため、依然としてブリスタリングの懸念が残ります。
では、この“内部”での現象にどう対処すべきでしょうか。
それが次に紹介する、再結合層という考え方です。
新たな対策:再結合層という発想
ブリスタリングは、水素ラジカルが再結合して生成されることによってガスが膨張します。
先ほどの2層構造では、この再結合が保護層内部で生じたために保護層第1層でブリスタリングが生じる可能性がありましたが、この再結合を保護層内部で無く、保護層表面で意図的に生じさせると、課題の解決が見えてきます。
水素が拡散して問題となる前に、保護層の第3層(以下の図中59:濃いピンクで示された層)で、水素ラジカル同士を再結合させて気体として外部に脱離させることができます。
この対策は、拡散前にラジカルを再結合させて排出することで、水素ラジカルの侵入自体を未然に防ぎます。
感染対策に例えると、「水素を持ち込まない、拡げない」設計とも言えます。
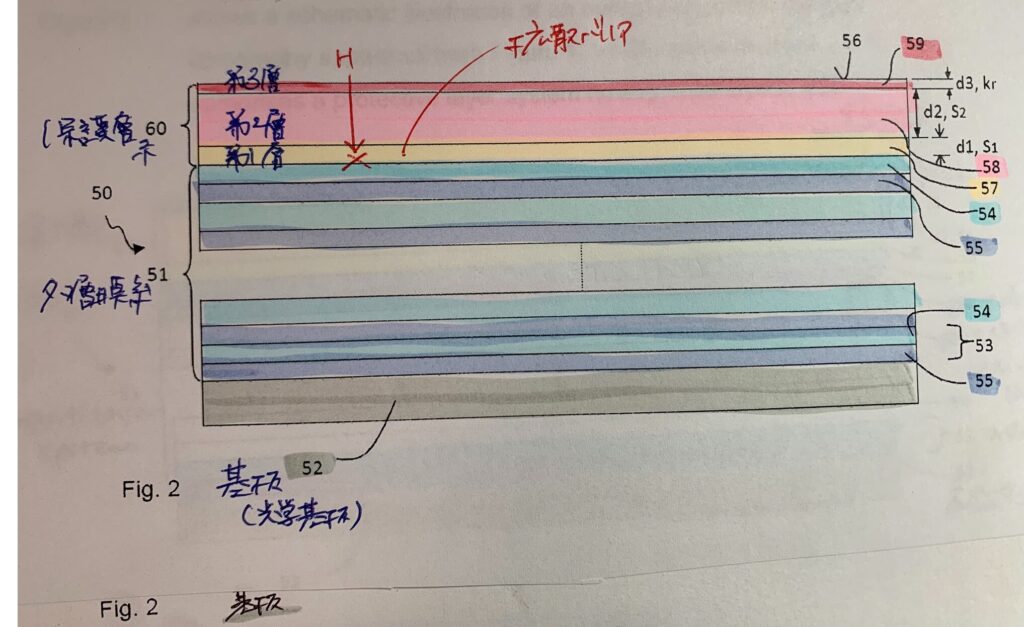
明細書では以下の箇所です。
In order that the diffusion of hydrogen into the protective layer system by the route described above is prevented to the greatest possible extent, the inventors propose producing a third, topmost layer of the protective layer system from a material which has a high recombination rate for hydrogen.
(参照自力翻訳:上記の経路により水素が保護層系に拡散するのを可能な限り防止するために、発明者らは、水素の再結合率が高い材料を用いて、保護層系の第3層すなわち最上層を形成することを提案する。)
材料特性:遷移金属
水素ラジカルを再結合させるのに、本明細書では、Mo, Ru, Pdなどの遷移金属やその酸化物の利用が提案されています。
以前「触媒反応」の記事で、金属表面に物理吸着したH₂分子がラジカルに解離する反応ステップについて書きましたが、今回の再結合層では、その逆の反応が生じていると考えられます。
金属触媒によって水素ラジカルに解離する場合、H₂分子はまず金属表面に吸着し、H-H結合が伸びた中間状態を経て、最終的に2つの水素ラジカルに分かれました。この際、金属表面は中間反応体を一時的に保てる場として機能します。
今回の再結合層では、互いに水素ラジカル同士が一時的に近接し、再結合するための場を提供する役割を果たします。
このような場を形成できるのが、d軌道に不対電子を持つ遷移金属です。d軌道がラジカル(不対電子)と電子的に相互作用することで、ラジカルを必要以上に引き寄せず、適度な吸着状態を維持し、中間体をエネルギー的に安定させます。これにより、ラジカル同士が近接した状態を保ちやすくなり、水素への再結合が進みやすくなります。
参考:
遷移元素の電子配置:https://pigboat-don-guri131.ssl-lolipop.jp/C%20Electronic%20configuration%20of%20transition%20elements.html
ケムステ:遷移金属と金属錯体~理論編~https://www.chem-station.com/yukitopics/complex.htm
表面構造:結晶性
さらに、表面に欠陥が多いと、結合後の水素分子が表面に再度引っかかりやすくなり、再吸着されやすくなってしまいます。
そのため、第3層では結晶性が高く、緻密で滑らかな表面(単結晶)が推奨されています。
おわりに
今回の明細書翻訳を通じ、発明の各態様や実施形態の位置付とその関係性の整理に多くの時間を費やしましたが、今回、それぞれに、何を変更して(構成)、何ができるようになったのか(機能)、代替手段なのか補完手段なのか、など視点を取り入れるのがよいのかなと思いました。
次の翻訳では重みづけを意識して翻訳を進めようと思います。



コメント